JUNTENDO News&Events ニュース&イベント
2024.03.19 (TUE)
- 順天堂大学について
- 研究活動
- メディアの方へ
- 企業・研究者の方へ
- 医学部
- 医学研究科
分子標的型抗がん剤による皮膚障害のメカニズムの一端を解明 ― 手足症候群などの皮膚障害の新規治療法開発に役立つ可能性 ―
順天堂大学大学院医学研究科環境医学研究所・順天堂かゆみ研究センターの髙森建二 所長、鎌田弥生 准教授らと東レ株式会社の共同研究グループは、がんの治療に用いられる分子標的型抗がん剤*1の副作用として見られる皮膚障害の発症機序の一端を解明し、その細胞障害を抑制する薬剤を発見しました。
分子標的型抗がん剤は従来の抗がん剤で見られる脱毛、骨髄抑制、吐き気などの副作用が少ない反面、ニキビのようなざ瘡様皮疹、爪の周りに炎症を起こす爪囲炎、皮膚の乾燥、手掌や足底に生じる手足症候群*2など、皮膚に副作用が生じやすいことが知られています。しかしながら、その発症機序はよくわかっておらず、主な治療法は対症療法のみでした。研究グループは分子標的薬のマルチキナーゼ阻害薬*3の一種であるソラフェニブ*4を用いて、約1200種類の既存医薬品のスクリーニングを行った結果、複数の薬が表皮角化細胞の細胞障害を抑制することを発見しました。本成果は、従来、発症機序もわからず、明確な治療法がなかったマルチキナーゼ阻害薬による手足症候群などの皮膚障害に対し、新規治療法開発の可能性を示すものです。
本論文はJID Innovations誌のオンライン版に2024年2月27日付で公開されました。
本研究成果のポイント
- 既存薬ライブラリー*5を用いて皮膚障害を抑制する薬剤のスクリーニングを実施
- いくつかの既存薬がソラフェニブによる表皮細胞障害を抑制することを発見
- 分子標的型抗がん剤による皮膚障害の新しい治療法の開発の可能性を示す
■背景
分子標的型抗がん剤はがん細胞の増殖・転移に関わる特定の分子を狙い撃ちすることから、従来の殺細胞性抗がん剤で見られるような脱毛、骨髄抑制、吐き気などの副作用が軽減することが知られています。しかしながら、分子標的型抗がん剤に特有の副作用としてざ瘡様皮疹、爪囲炎、皮膚の乾燥、手掌や足底に生じる手足症候群などの皮膚障害が認められることがあり、その副作用は生命に影響しないものの、見た目やかゆみ、歩けないほどの痛みなどにより、患者さんの生活の質は著しく低下します。その治療法はステロイド剤や保湿剤の塗布などの対症療法に限られており、なぜ副作用として皮膚障害が起きるのか、どうすれば症状を軽減できるのかは不明でした。そこで、今回、研究グループは分子標的型抗がん剤の一種であるマルチキナーゼ阻害薬のソラフェニブによる手足症候群に注目し、その発症メカニズムの解明と新規治療法を開発することを目的に、既存薬ライブラリーのスクリーニングを行い細胞保護剤の探索と、その作用機序の解明を行いました。
■内容
本研究は、ドラッグリポジショニング*6を目指し、約1200種類の既存医薬品から構成されるライブラリーを用いて、ソラフェニブによる表皮細胞毒性を軽減する薬剤をスクリーニングしました。培養した正常ヒト表皮角化細胞*7に7 μMのソラフェニブと1 μMの各薬剤を添加し、一晩培養後、細胞生存率を解析した結果、ソラフェニブによる細胞毒性を有意に抑えた薬剤が15種類同定されました。二次スクリーニングとして、三次元培養ヒト表皮モデルの培地にソラフェニブと各薬剤を添加し、4日間培養後に細胞生存率を解析した結果、クロファジミン*8、シクロスポリンA*9、イトラコナゾール*10、ピルビニウムパモ酸塩*11の4種類が有意に細胞毒性を抑えることが判明しました。増殖細胞のマーカーである増殖細胞核抗原(PCNA)の発現を免疫組織化学染色で解析したところ、溶媒群と比べてソラフェニブ群ではPCNA陽性細胞数は減少し、クロファジミン、シクロスポリンA、イトラコナゾールといった候補薬を添加すると、PCNA陽性細胞数は有意に増加しました。また、アポトーシス*12をアネキシンV染色で検出したところ、ソラフェニブ群は溶媒群と比べてアポトーシス細胞が増加しており、候補薬を添加するとアポトーシス細胞の増加が抑制されました。さらに、ソラフェニブの阻害標的となるRafキナーゼの下流に位置するシグナル分子ERK1/2*13の活性化(リン酸化)状態を解析した結果、ソラフェニブ群は溶媒群と比べてERK1/2のリン酸化が阻害されており、クロファジミン、イトラコナゾール、ピルビニウムパモ酸塩などの候補薬を同時に添加することで、そのリン酸化阻害が解除されることがわかりました。
以上のことより、これらの候補薬はソラフェニブによるERK1/2のリン酸化阻害を解除し、アポトーシスを抑制、細胞増殖を正常化することで表皮角化細胞に対する細胞保護作用を発揮するものと考えられます。
■今後の展開
今回、研究グループは発症メカニズムが不明で治療法も対症療法だけであった、分子標的型抗がん剤による手足症候群の発症メカニズムの一端を解明し、治療薬の候補となる物質を発見しました。このたびの研究はすべてin vitro*14で実施されたため、実用化に当たってはさらに基礎と臨床をつなぐトランスレーショナルリサーチ(橋渡し研究)が必要です。今回、同定した候補薬は既に国内で承認され医療に用いられている既存薬であることから、早期に新規治療法として応用できる可能性があります。特にイトラコナゾールと同系統のアゾール系抗真菌薬は外用薬もあり、皮膚科領域で汎用されていることから、研究グループでは倫理委員会の承認を得た上で、抗真菌薬クリームの手足症候群への治療効果について臨床試験を進めています。皮膚に塗布する外用剤であれば、がん治療に支障をきたす可能性が少ないことから、本治療法が適用されれば、既存の外用薬により手足症候群の症状が軽減し、がん治療中の患者さんの生活の質が向上することが期待されます。今回、候補薬は共通してアポトーシス阻害作用を示しましたが、細胞増殖促進作用やERK1/2リン酸化の正常化作用は候補薬により、違いがあったため、個々の候補薬の細胞保護メカニズムに関しても解析を進めて行きます。
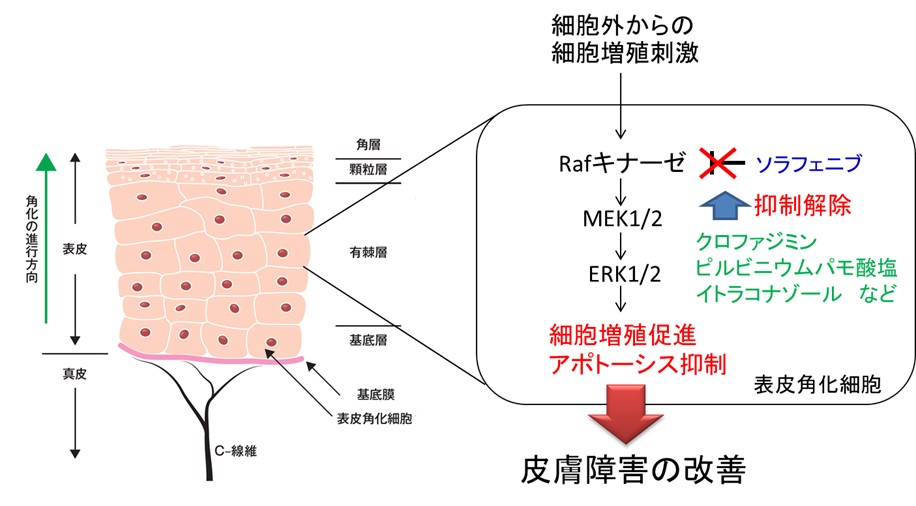
図1:本研究で明らかになった手足症候群の発症メカニズムと治療薬の作用点
健康な表皮角化細胞の増殖と分化を制御しているシグナル伝達経路の一つにMAPK-ERK経路があります。細胞外からの細胞増殖因子などのシグナルを受けとると、Rafキナーゼ、MEK1/2を介してERK1/2がリン酸化され、最終的に細胞の増殖、分化、生存などが制御されます。ソラフェニブの作用点の一つにRafキナーゼの阻害があり、下流のシグナル伝達が阻害されることで、細胞増殖阻害やアポトーシスが起きると考えられます。今回発見した候補薬のうち、クロファジミン、ピルビニウムパモ酸塩、イトラコナゾールは表皮角化細胞におけるERK1/2のリン酸化を回復させることがわかりました。それにより、アポトーシスを抑制し、細胞増殖を回復させたものと考えられます。
■用語解説
*1 分子標的型抗がん剤:がん細胞に特有のタンパク質などを狙い撃ちすることで効果を示す薬剤。
*2 手足症候群:抗がん剤治療中に手や足に見られる紅斑、水ぶくれ、痛みなどの一連の症状のこと。
*3 マルチキナーゼ阻害薬:がん細胞の増殖・転移に関わる複数のリン酸化酵素の働きを阻害する薬剤。
*4 ソラフェニブ:マルチキナーゼ阻害薬に分類される薬剤の一種。
*5 既存薬ライブラリー:日本や海外で承認されている医薬品を集めたもの。
*6 ドラッグリポジショニング:ヒトにおける体内動態や安全性が既に明らかにされている既存薬の新しい薬効を見出して、別の疾患治療薬に応用すること。
*7 表皮角化細胞:皮膚の最外層である表皮を構成している細胞。
*8 クロファジミン:ハンセン病治療薬
*9 シクロスポリンA:免疫抑制剤
*10 イトラコナゾール:アゾール系抗真菌薬
*11 ピルビニウムパモ酸塩:寄生虫駆虫薬
*12 アポトーシス:細胞が自ら死に向かう、プログラムされた細胞死のこと。
*13 ERK1/2:細胞外の様々な刺激に応答して、細胞の増殖、生存、分化などに関わるリン酸化酵素の一種。
*14 in vitro:生体を使用しない、試験管や培養器内での研究。
■原著論文
本研究は米国研究皮膚科学会と欧州研究皮膚科学会発行の学術雑誌JID Innovations誌のオンライン版に2024年2月27日付で公開されました。
タイトル: Identification of keratinocyte cytoprotectants against toxicity by the multikinase inhibitor sorafenib using drug repositioning
タイトル(日本語訳): ドラッグリポジショニングによるマルチキナーゼ阻害薬ソラフェニブの細胞毒性に対するケラチノサイト細胞保護剤の同定
著者:Yayoi Kamata, Rui Kato, Mitsutoshi Tominaga, Sumika Toyama, Eriko Komiya, Jun Utsumi, Takahide Kaneko, Yasushi Suga, Kenji Takamori
著者(日本語表記): 鎌田弥生1,2)、加藤塁1,3)、冨永光俊1,2)、外山扇雅1)、古宮栄利子1)、内海潤1)、金子高英3)、須賀康2,3)、髙森建二1,2,3)
著者所属:1)順天堂大学大学院医学研究科環境医学研究所・順天堂かゆみ研究センター、2)順天堂大学大学院医学研究科抗加齢皮膚医学研究講座、3)順天堂大学医学部附属浦安病院皮膚科
DOI:https://doi.org/10.1016/j.xjidi.2024.100271
本研究は東レ株式会社との共同研究ならびにマルホ奨学寄付支援プログラム(2021-2023年度)の支援の基に実施されました。また、本研究成果の一部は令和5年7月に特許を取得しています(抗がん剤投与により生じる皮膚障害の治療または予防剤、特許第7315167号)。本研究にご協力いただいた皆様には深謝いたします。