JUNTENDO News&Events ニュース&イベント
2025.08.26 (TUE)
- 順天堂大学について
- 研究活動
- メディアの方へ
- 企業・研究者の方へ
- 医学部
- 医学研究科
切除不能進行膵癌に対するWT1標的免疫化学療法における長期生存例に基づいた治療効果予測バイオマーカーの探索的研究
順天堂大学大学院医学研究科腸内フローラ研究講座の特任教授 佐藤信紘と特任教授 大草敏史は、東京慈恵会医科大学の消化器・肝臓内科教授(当時)
本研究の成果は、2025年7月31日にJournal for ImmunoTherapy of Cancer誌オンライン版に掲載されました。
本研究のポイント
- 外科切除不能と判断された進行膵癌10例に「WT1標的免疫化学療法」を実施したところ、7例が縮小ないし長期間安定し手術が可能となりました。
- そのうち4例は5年以上の長期生存が可能となり、3例は再発・転移なく現在でも6年以上の生存を維持しています。
- 長く生存された方では、治療効果予測バイオマーカーとして、治療前からWT1に反応する免疫の働き(免疫応答)がすでに備わっていることが判明しました。
- 特に、膵癌細胞を繰り返し攻撃できる「WT1特異的記憶型のCD8+T細胞(セントラルメモリーCD8+T細胞)」が増えていたことがわかり、これが長期生存に関係している可能性が示されました。
- 「WT1標的免疫化学療法」では、WT1以外にも膵癌細胞が持つ様々な目印(腫瘍抗原)に対しても免疫応答が誘導されることが確認されました。
- 治療前からWT1に対する免疫応答を有している場合は「WT1標的免疫化学療法」が有望な治療戦略となる可能性を見出しました。
【今後の展望】
本臨床試験では、切除不能進行膵癌10例を対象に、「Neo-WT1樹状細胞」(計15回)と抗癌剤(ナブパクリタキセルとゲムシタビン:Nab-P/Gem)との併用治療である「WT1標的免疫化学療法」を実施しました。今後は、化学療法単独治療群などの比較対照を含む大規模な臨床試験や治験により、本治療法の有効性と安全性を検証することが重要です。
【論文情報】
掲載誌:Journal for ImmunoTherapy of Cancer誌オンライン版
論文タイトル:Predictors of patients with advanced pancreatic cancer undergoing conversion surgery via chemoimmunotherapy with a multifunctional Wilms' tumor 1 (WT1) peptide cocktail-pulsed dendritic cell vaccine
著者:Shigeo Koido, Junichi Taguchi, Masamori Shimabuku, Tuuse Bito, Soyoko Morimoto, Yusuke Oji, Yoshihiro Oka, Masaki Ito, Yoko Shimizu, Zensho Ito, Kan Uchiyama, Masayuki Saruta, Nobuhiro Sato, Toshifumi Ohkusa, Shigetaka Shimodaira, Haruo Sugiyama
DOI:10.1136/jitc-2024-011426
掲載URL: https://jitc.bmj.com/content/13/7/e011426
本研究はJSPS科研費の助成をうけたものです。
【協力メンバー(氏名・研究実施時の所属)】
小井戸 薫雄 ・東京慈恵会医科大学附属柏病院 消化器・肝臓内科
田口 淳一 ・東京ミッドタウン先端医療研究所
島袋 誠守 ・東京ミッドタウン先端医療研究所
尾藤 通世 ・東京慈恵会医科大学附属柏病院 消化器・肝臓内科
森本 創世子・大阪大学大学院医学系研究科 癌幹細胞制御学寄附講座
尾路 祐介 ・大阪大学大学院医学系研究科保健学専攻 生体病態情報科学講座
岡 芳弘 ・大阪大学大学院医学系研究科 癌幹細胞制御学寄附講座
伊藤 正紀 ・東京慈恵会医科大学 総合医科学研究センター 臨床医学研究所
清水 洋子 ・東京ミッドタウン先端医療研究所
伊藤 善翔 ・東京慈恵会医科大学附属柏病院 消化器・肝臓内科
内山 幹 ・東京慈恵会医科大学附属柏病院 消化器・肝臓内科
猿田 雅之 ・東京慈恵会医科大学 消化器・肝臓内科
佐藤 信紘 ・順天堂大学大学院医学研究科 腸内フローラ研究講座
大草 敏史 ・東京慈恵会医科大学附属柏病院 消化器・肝臓内科 / 順天堂大学大学院医学研究科 腸内フローラ研究講座
下平 滋隆 ・金沢医科大学 再生医療学講座
杉山 治夫 ・大阪大学大学院医学系研究科 癌免疫学寄附講座
■研究の詳細
背景
進行膵癌は、体の免疫が働きにくい特別な環境を癌の周囲につくってしまうため、これまでの化学療法、放射線療法および免疫の働きを助ける薬(免疫チェックポイント阻害剤)が効きにくいことがあります。しかし最近では、この癌周囲の環境(腫瘍微小環境といいます)そのものを治療の標的とする「免疫化学療法」という新しい治療法が注目されており、手術ができない膵癌の方にも新たな治療の選択肢として期待されています。
WT1は、膵癌細胞、癌の根元となる細胞(癌幹細胞)、癌に栄養を送る血管、さらに免疫の働きを抑える細胞にも多く発現していることがわかっています。そのため、WT1は様々な癌に対する治療の標的として注目されています。私たちは、これまでのWT1とは異なる新しいタイプのWT1(Neo-WT1)ペプチドを用いて、免疫を活性化させる細胞(樹状細胞)にNeo-WT1の情報を与えて、膵癌の方に投与する「Neo-WT1樹状細胞療法」を開発しました。これを、現在使われている化学療法(ナブパクリタキセルとゲムシタビン:Nab-P/Gem)と組み合わせた「WT1標的免疫化学療法」を、世界に先がけて考案・実施してきました(下図)。
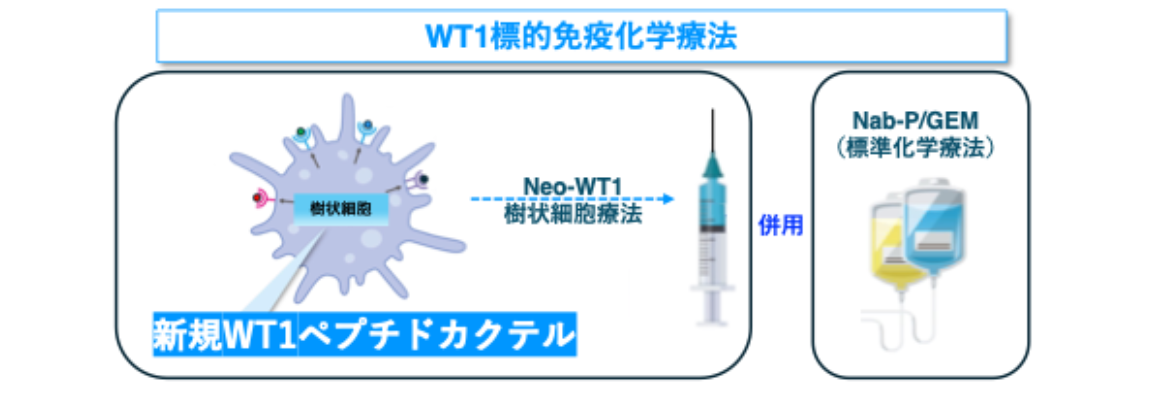
この治療法は、WT1という癌の目印に対して強い免疫の働きを引き出すことができ、手術が不可能な進行膵癌の方でも、癌を完全に取り切る手術(R0切除)が可能になった方もおられました。ただし、「WT1標的免疫化学療法」の効果には、それぞれの免疫反応など、様々な要因が関係していると考えられています。そのため、この治療が誰にどのように効くかを正確に予測することは、困難でした。
<WT1標的免疫化学療法の治療スケジュール>
1コース目は標準化学療法(ナブパクリタキセルとゲムシタビン:Nab-P/Gem)のみを使用し、2コース目から「Neo-WT1樹状細胞」と標準化学療法(Nab-P/Gem)を併用しました。「Neo-WT1樹状細胞」の投与は15回に限定しました(下図)。
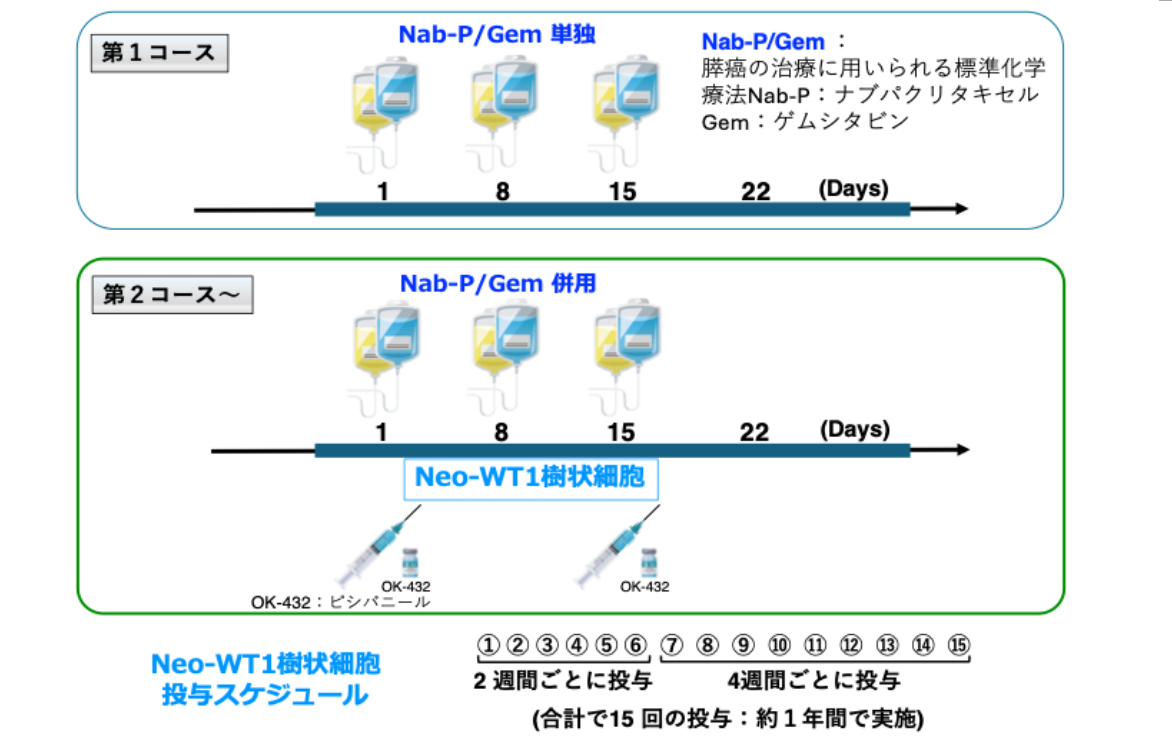
目的・手技
多くの膵癌細胞には、WT1という「たんぱく質」が発現しています。このWT1をねらって攻撃する「免疫療法」と、抗癌剤を組み合わせた治療法を「WT1標的免疫化学療法」といいます。この新規治療法がどれくらい効果があるのかを予測するために、私たちは体の中でどのような変化が起きているか、また癌の状態がどうなっているかを詳しく調べました。今回は、当初には手術ができなく進行膵癌9例を対象に、次のことを調べました。
- WT1に反応して癌を攻撃する免疫細胞(キラーCD8+T細胞)のうち、再び癌に出会ったときにすぐに働ける「WT1特異的セントラルメモリーCD8+T細胞」がどのくらい存在するか
- WT1を発現している癌を攻撃する「WT1抗体」が、どのくらい体の中にあるか
- 癌のまわりに集まっている免疫細胞の種類や数はどうか
- 血液の中に流れている癌細胞の循環腫瘍DNA(ctDNA)にどのような変化があるか
- 膵癌細胞そのものが、どのような特徴を持っているか
これらの情報をもとにして、「WT1標的免疫化学療法」がどのような方に効果が出やすいのかを明らかにすることが、本研究の目的です。
成果
治療成績
切除不能進行膵癌9例における無増悪生存期間および全生存期間の中央値は、それぞれ、2.23年と3.52 年でした (下図)。
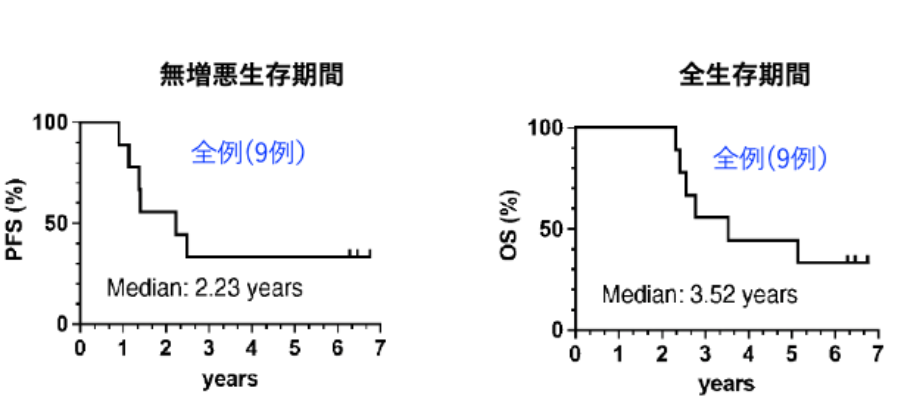
膵癌が縮小ないし安定後に手術が可能であった方(7例)は、手術ができなかった方(2例)と比較し、長期間の生存が認められました。手術が可能であった4例は5年以上生存しました。また、3例では6年経過後も再発や転移を認めていません。長期生存された方は、局所進行切除不能膵癌で、WT1に特異的な免疫反応が強く誘導できた結果、手術が可能となった方でした(下図)。
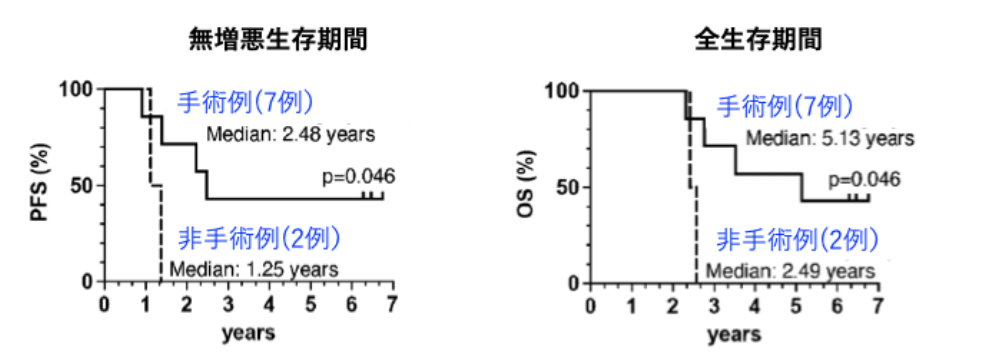
(2)治療効果予測バオマーカー
長期生存をきたした方は、治療成績がやや劣った方と比較し、次のような特徴を有していました。
1.末梢血中のWT1特異的CD8+ナイーブT細胞数が治療前の段階で減少していました。
2.WT1に対するIgM抗体量が治療前から多くみられました。
3.治療前の血液中に、変異を示した癌遺伝子(KRAS・TP53など)が見られませんでした。
4.治療前から血液中ctDNAに変異が見つかった方は、治療後にその頻度が減少しました。
5.膵癌細胞がPD-L1というたんぱく質を多く発現していない方は、長期生存されました。PD-L1は、免疫細胞の働きを「ブレーキ」する役割があり、これが少ないと免疫が効きやすくなります。
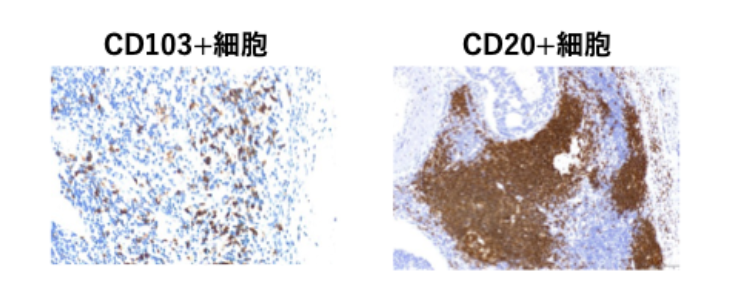
6.膵癌のまわりの組織(腫瘍微小環境)を詳しく見たところ、治療効果が高かった方では、CD103+細胞(以下左図の茶色い細胞)やCD20+細胞(以下右図の茶色い細胞)という免疫細胞が多く集簇していましたが、今回の解析では生命予後との関連は認められませんでした。
7.特に治療効果が高かった方では、治療後にWT1特異的セントラルメモリーCD8+T細胞数が末梢血中で増加していました。
このように、「WT1標的免疫化学療法」の効果が高い方は、治療前からWT1に対して免疫応答の準備が整っている状態でした。治療前や治療経過中に、これらの特徴を調べることで、誰にこの治療が有効であるかを予測できるようになるかもしれません。
今後の応用、課題
今後、「WT1標的免疫化学療法」の効果を正確に確かめるためには、化学療法だけの治療や、免疫療法だけの治療を比較対象(コントロール)とした大規模な臨床試験や治験を行うことが望まれます。こうした研究を通じて、「WT1標的免疫化学療法」が本当に他の治療よりも効果的かどうかを科学的に検証することができます。また、この治療が特に効果を発揮しやすい方を見つけ出すためのバイオマーカーの開発も非常に重要です。たとえば、治療を始める前から、(1)WT1に反応する免疫細胞(T細胞)がすでに活性化している方や(2)WT1に対する抗体が作られている方では、この治療法によく反応する可能性があると考えられます。こうした予測に関しても、本当に正しいかどうかを証明するには、さらに多くの方を対象とした比較試験や治験が必要であり、今後の大きな課題です。
要約
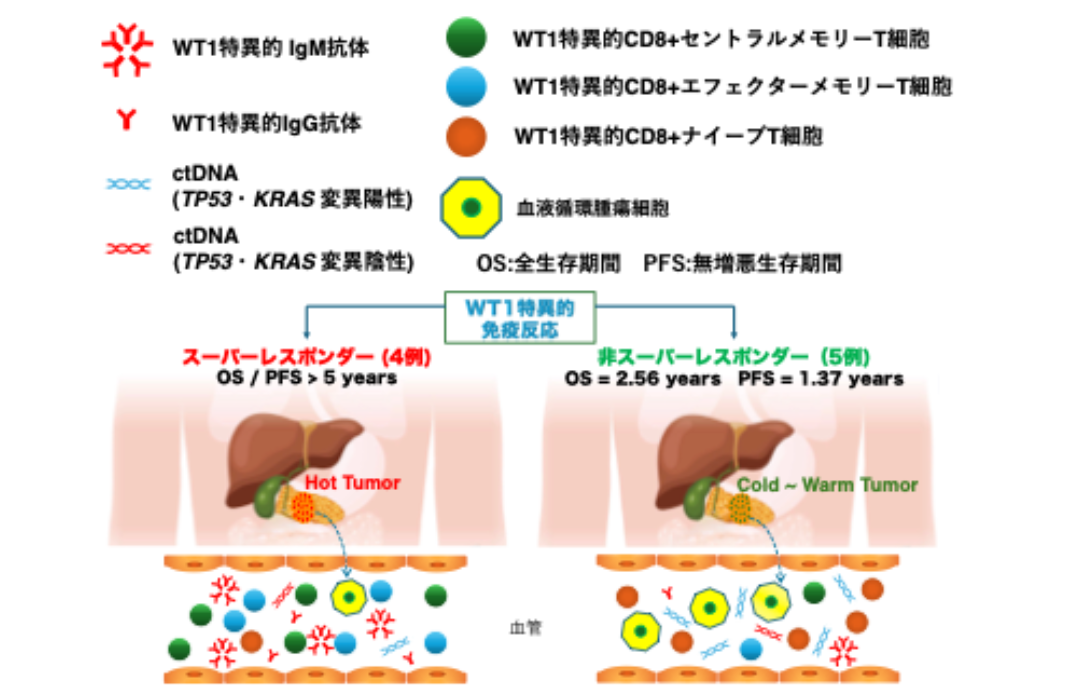
「WT1標的免疫化学療法」にて優れた治療成績が得られた「スーパーレスポンダー」と治療成績がやや劣った「非スーパーレスポンダー」におけるWT1特異的免疫反応の相違について、要約図を以下に示します。
【要約図】
(要約図の説明)
- 膵癌の多くは腫瘍微小環境において免疫細胞、特にT細胞がほとんど存在しない、または免疫応答が抑制されている腫瘍(cold tumor)がほとんどですが、「WT1標的免疫化学療法」にて一部の腫瘍は免疫が活性化した腫瘍(hot tumor)に変換できる可能性があります。
- 治療前の時点でWT1特異的CD8+ナイーブT細胞の数が少なく、WT1特異的IgM抗体のレベルが高い方は、「WT1標的免疫化学療法」の恩恵を受ける可能性があります。
- 「WT1標的免疫化学療法」のスーパーレスポンダーでは、非スーパーレスポンダーよりも有意に多くのWT1特異的セントラルメモリーCD8+T細胞が治療後に増加しました。
- 治療前に、血中の循環腫瘍DNA(ctDNA)中に、2つの主要遺伝子(KRASとTP53)のいずれかの変異(すなわち、ネオアンチゲン)があり、PD-L1を高レベルで発現している膵癌細胞がある方は、予後が有意に不良でした。
- 化学療法や「Neo-WT1樹状細胞療法」により膵癌が破壊された後、様々な腫瘍抗原が放出されます。その結果、ネオアンチゲンやオンコアンチゲンに反応する「IFN-γを産生するCD8+T細胞」の誘導を確認することができました(下図の下段に示した青色矢印)。すなわち、「WT1標的免疫化学療法」では、ネオアンチゲン(変異のあるTP53など)とよばれる癌細胞特有の異常たんぱく質や、オンコアンチゲン(WT1やTP53やKRASなど)にも反応する免疫が誘導されることを確認しました。したがって、この治療により、ネオアンチゲンやオンコアンチゲンを発現している膵癌細胞を免疫が認識し、攻撃・排除することが期待されています。つまり、様々なネオアンチゲンやオンコアンチゲンという「癌の目印」にも反応することで、より強力な癌攻撃の仕組みが働いている可能性があります(下図)。
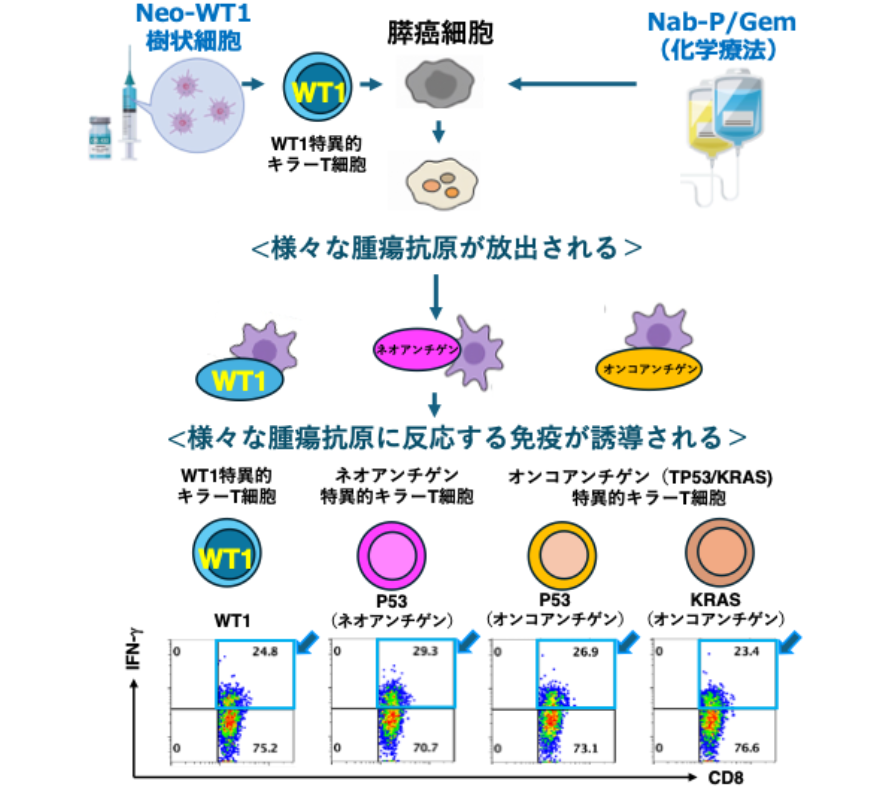
最下段の青色矢印:ネオアンチゲンやオンコアンチゲンに反応する「IFN-γを産生するCD8+T細胞」の誘導を確認することができました。
脚注、用語説明
(1) WT1
WT1とは、癌細胞が持つ特有な目印のようなもので、白血病、肺癌、大腸癌、膵癌、さらには骨や筋肉の腫瘍、脳腫瘍など、様々な腫瘍に発現しているたんぱく質の一つです。また、WT1は癌の元になる「癌幹細胞」や、癌のまわりに集まって癌を助ける「マクロファージ」や「癌に栄養を送る血管」にも見られます。そのため、WT1を狙って治療することで、いろいろな角度から癌を攻撃できる可能性があり、治療効果への期待が高まっています。
(2) Neo-WT1樹状細胞
免疫療法は、体に本来備わっている「免疫の力」を利用して、癌細胞を攻撃する治療法です。癌細胞には、体の正常な細胞にはあまり見られない「癌特有の目印」がたくさんあります。この目印となる物質は「腫瘍抗原」と呼ばれています。免疫療法では、WT1のような「腫瘍抗原」だけを狙って攻撃できるように体の免疫を強く働かせます。そのため、正常な細胞にはあまり影響せず、副作用が少ない治療法と考えられています。癌細胞を攻撃する主な免疫の働き手は「リンパ球」です。「リンパ球」を強く働かせるために活躍するのが、「樹状細胞」という細胞です。樹状細胞は、リンパ球に「この細胞が癌だから攻撃しなさい」と教える司令官のような役割を果たします。今回の治療では、「Neo-WT1」という新しいタイプのWT1たんぱく質の断片(ペプチド)を2種類、「樹状細胞」にパルスしたもの(「Neo-WT1」を覚え込ませたもの)を、「Neo-WT1樹状細胞」として使用しています。「Neo-WT1樹状細胞」は、従来の「WT1樹状細胞」と比べて、より強く癌を攻撃できるように、「リンパ球」をトレーニングできる可能性があり、更に良好な治療効果が期待されています。
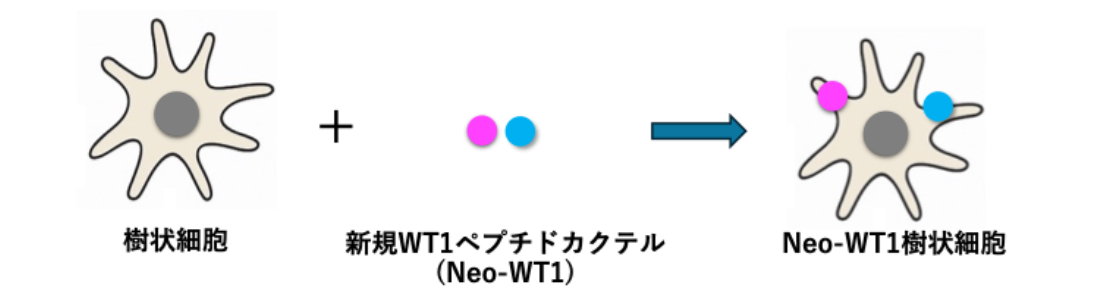
「Neo-WT1樹状細胞」にてトレーニングを受けた「リンパ球」は、「WT1」という目印をもつ膵癌細胞を見つけて攻撃できる「強い戦う細胞」になります。ただし、どれくらい強く、どのくらいの期間その免疫が働くかには個人差があります。長くしっかりと免疫が効く方もいれば、反応が弱い方もいました。しかし、膵癌の多くで「WT1」という目印が発現しているため、多くの方が「Neo-WT1樹状細胞」が使える可能性があります。
(3) 無増悪生存期間(PFS: Progression-Free Survival)
無増悪生存期間とは、診断や治療開始から病状が悪化せずに生存している期間です。
(4) 全生存期間(OS: Overall Survival)
全生存期間とは、診断や治療開始からあらゆる原因で死亡するまでの期間です。
(5) ナイーブT細胞
ナイーブT細胞とは、まだ本格的に働いたことのない「新人」の免疫細胞です。ナイーブT細胞の数が少ないということは、すでに免疫の「経験者」が多い可能性があります。
(6) IgM抗体
IgM抗体とは、体が最初に作る抗体です。これが多いと「敵(すなわち癌)が来た」というサインにすばやく反応できます。
(7) 血中腫瘍DNA
血中腫瘍DNAとは、癌細胞から出て血液中を流れている癌の遺伝子(DNA)の断片です。
(8) ネオアンチゲン
ネオアンチゲンとは、癌細胞が突然変異によって作り出した、まったく新しい「癌の目印」のようなものです。
(9) オンコアンチゲン
オンコアンチゲンとは、癌細胞だけが持っている特別な「癌の目印」のようなものです。WT1はオンコアンチゲンの一つとして知られています。
ネオアンチゲンやオンコアンチゲンなどの「癌の目印」を、特別な免疫細胞が見つけることで、癌細胞を攻撃することができるようになります。
(10) CD103+細胞
CD103+細胞とは、癌のある場所にとどまって、攻撃し続ける免疫細胞です。
(11) CD20+細胞
CD20+細胞とは、B細胞に発現しており、抗体を作る手助けをします。