花粉症の季節になると鼻だけでなく、眼のかゆみに悩まされる人も多いでしょう。順天堂大学大学院医学研究科アトピー疾患研究センターの安藤智暁准教授らの研究グループは、花粉に由来するアレルギー性結膜炎の発症メカニズムの解明を通して、眼の粘膜がアレルゲンを能動的に取り込む機構を明らかにしました。この研究成果は、花粉症だけでなく、さまざまなアレルギー疾患の病態理解と治療への応用を促進する可能性を秘めています。
アレルギー疾患が引き起こされる原因とは?

現代社会においては、実に多くの人々が花粉症(
注射や食物摂取などで全身にアレルギー反応が生じることもありますが、多くの場合、アレルギー疾患が起きる体の部位は体の表面になります。私たちが注目しているのは、濡れた状態に保たれている「粘膜」というタイプの組織です。私たちヒトは、水生生物から進化してきたと考えられています。そのため皮膚以外の体の表面は、多かれ少なかれ濡れていることにより、その機能を発揮できるようにつくられています。例えば、眼は視機能を維持するために涙液によって濡れています。同様に、鼻腔や肺などの気道、腸の消化管なども体液によって濡れた状態が保たれています。
粘膜は皮膚に比べて柔らかいので、摩擦で破れてしまわないように、表面をつるつるに保つ「潤滑」の仕組みを備えています。一方、柔らかいながら、外からの異物を除去するためのバリア機能も備わっています。眼の表面でこの“つるつるバリア機能”を担っている主な細胞は2種類で、直接的なバリアを担う上皮細胞と、粘液を放出する杯細胞(Goblet Cell)です。私たちは、後者の杯細胞が、眼の粘膜における物質の取捨選択に関わる非常に重要な役割を担っていることを発見し、その研究を続けてきました。


眼が物質を取捨選択し能動的に取り込む機構を解明する
研究テーマは、「眼が物質を取捨選択し能動的に取り込む機構の解明」です。主に、アレルギー性結膜炎が引き起こされるメカニズムの解明を通して、眼の表面を保護する役割を担う杯細胞の役割を細かく調べています。ここにおける眼が物質を取捨選択する仕組みは、2つの段階から成り立っています。それは、①有害な存在をフィルターする段階、②フィルターされた物質を取り込む段階です。
まず①のフィルターに用いるのが、杯細胞の出す粘液です。私たちは、粘液の本体であるムチンタンパク質が、花粉など外来の粒子を粘液カプセルで閉じ込め、バクテリアなどの小さな有害粒子が出てこないようにする作用を持つことを発見しました。そして、その作用に、ムチンタンパク質表面のシアル化糖鎖が重要な役割を果たしていることを明らかにしました。この糖鎖を変えることにより、粘液タンパク質の性質をコントロールできれば、さらなる防御作用を加えることができるかもしれないと考えて研究を進めています。
さらに重要なのが、②の取り込む段階の研究です。これまでは、眼の粘膜のバリア機能が「低下する」ことよって、アレルゲン物質が受動的に取り込まれると考えられてきました。しかし、杯細胞は粘膜の外の物質を積極的に取り込み、粘膜内に放出する作用があることが私たちの研究で明らかになったのです。

研究キーワードは「杯細胞を介したGAP形成」
ここで研究のキーワードになるのが、goblet cell associated antigen passage (GAP)と呼ばれる杯細胞を通じた物質の取り込み経路です。これは、他の研究グループによって腸管で機能していることが報告されてきましたが、結膜においてはまったく別の仕組みで同様の現象が生じている可能性があります。私たちの研究グループは、マウスを用いた実験によって、花粉の殻による刺激が神経系を介して速やかにGAP形成を誘導することを明らかにしました。さらに、このGAPを介した能動的なアレルゲン取り込みが、花粉によるアレルギー性結膜炎の発症を引き起こすことを明らかにしました。
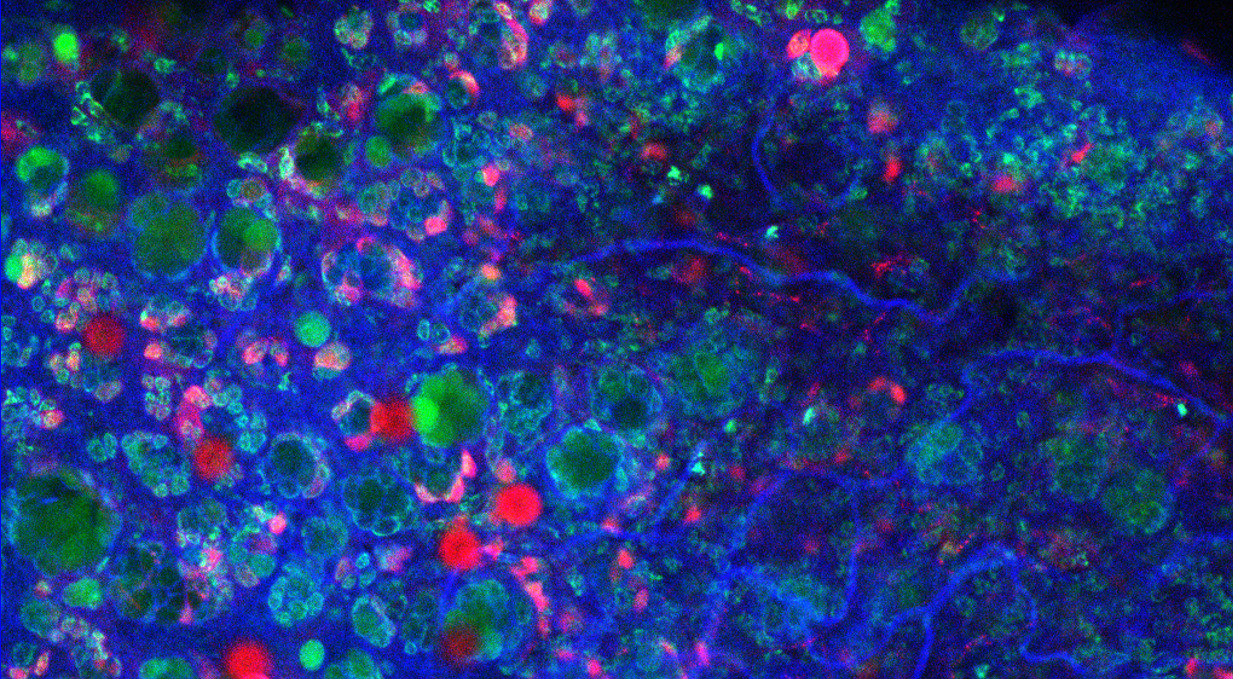
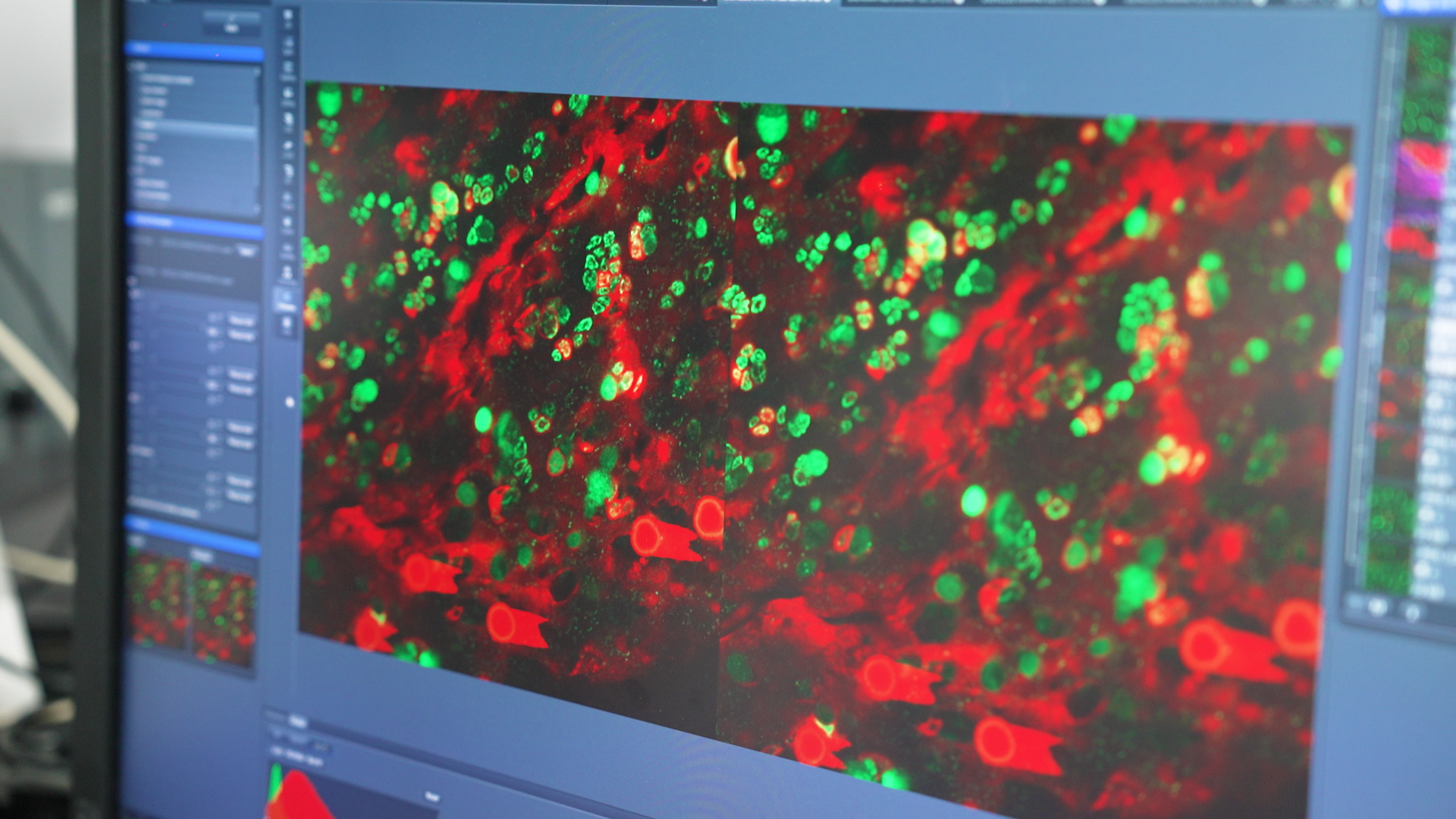
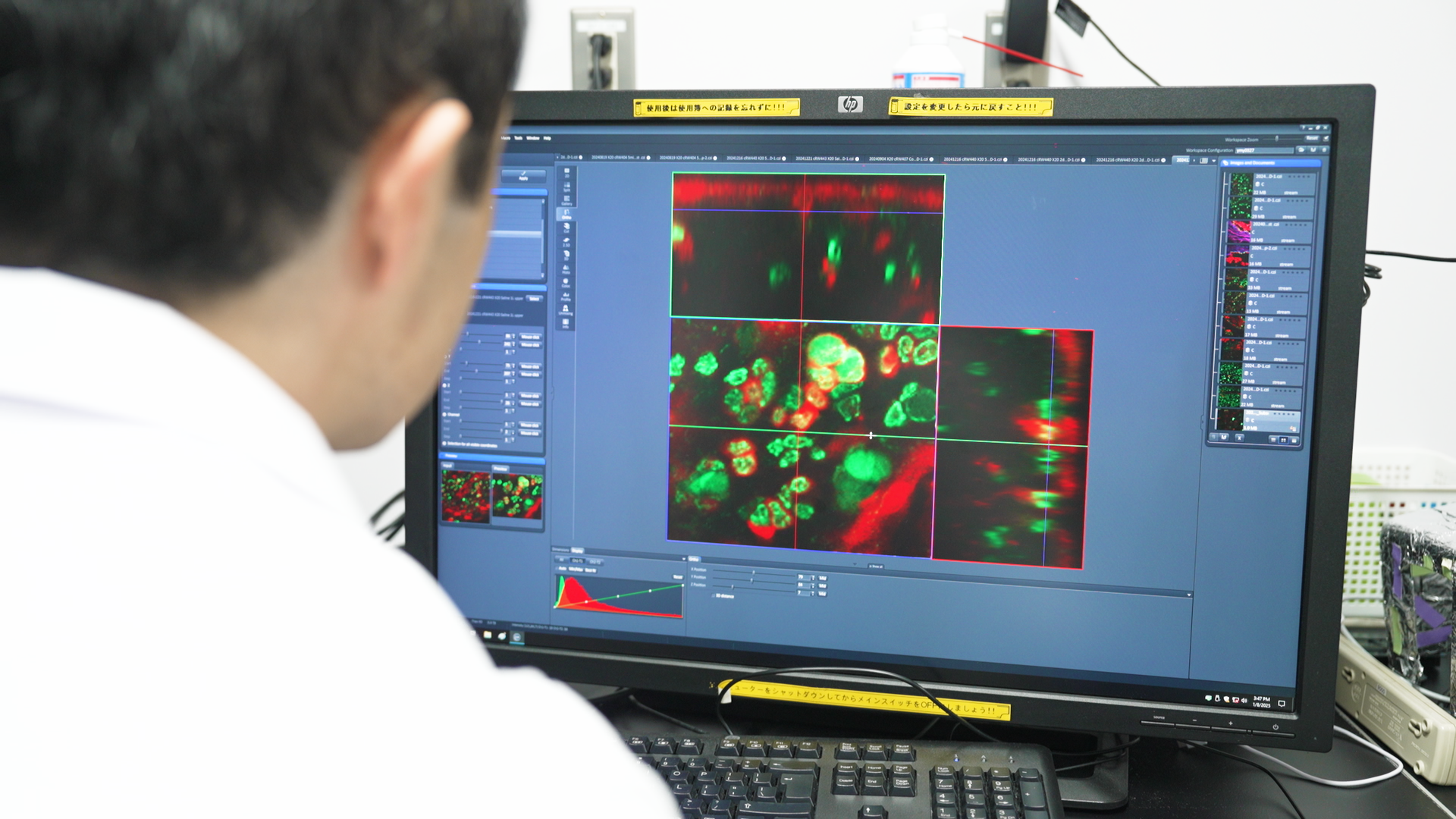
実験では、まずブタクサ花粉のエキスを蛍光色素で染色し、粘膜組織内でどのように分布するかを可視化しました。花粉のエキスのみを点眼した場合と花粉の殻とともに点眼した場合とを比較したところ、花粉の殻とともに点眼した場合には、杯細胞が細胞内に大量にアレルゲンを取り込み、その直下の免疫細胞に受け渡している様子が観察されました。この現象が、花粉の殻と蛍光アレルゲン(花粉エキス)を点眼してから5分以内という非常に短い時間で観察されたことから、杯細胞のGAP形成による能動的なアレルゲンの取り込みが、速やかなアレルギー症状発症に関与している可能性が示されたのです。
さらに、マウスを用いた別の花粉症モデル実験において、マウスに花粉を点眼した後眼を洗ってみたところ、10分後に洗眼したマウスと洗眼しなかったマウスとで、花粉症の発症レベルにほとんど差がないことが判明しました。つまり、花粉が眼に付着してすぐに、杯細胞のGAP形成によるアレルゲン取り込みがほぼ完了していることが明らかになったのです。
さらに、眼におけるGAP形成の仕組みを詳しく調べてみると、眼の表面で触覚などの感覚を司る三叉神経が重要な役割を担っており、神経を麻痺させるとGAPが形成されなくなることが判明しました。これらの仕組みの解明を進めることによって、アレルゲンの取り込みをブロックしたり、逆に利用して薬を取り込ませたりできないかと考えています。

アレルギー疾患の病態理解と治療への応用に期待
粘膜バリアが、単なる盾ではなく能動的な存在であるというパラダイムシフトは、粘膜を介した物質輸送をコントロールできるかもしれないという、新たな可能性を私たちに示しています。今回の杯細胞を介したGAP形成を含むアレルゲン取り込みの詳細なメカニズムはまだ解明されていません。しかし、これを明らかにすることで、アレルゲンの取り込みを阻止したり、逆に薬を取り込ませたりするといった可能性が広がります。
さらに、腸管における杯細胞と異なる仕組みで働いているということは、粘膜臓器特異的なコントロールができるかもしれないという可能性も示唆しています。今後、気道などの粘膜においても類似の現象がみられるのかどうかなどについても明らかにしていくことによって、粘膜バリアの理解を深め、アレルギー疾患の病態理解と治療への応用を促進していきたいと考えています。

研究者Profile

安藤 智暁
Tomoaki Ando
大学院医学研究科アトピー疾患研究センター
准教授
【関連記事】機序から治療まで4半世紀にわたってアトピー疾患の研究をリード
Researchmap