精神疾患の中でも頻度の高い双極性障害は、躁状態とうつ状態を繰り返すことから、社会生活への影響も大きい病気です。未だ原因が解明されていないこの病気について、医学部精神医学講座では、ゲノム解析やモデル動物を用いた実験などの多彩なアプローチで研究し、病態の核心に迫る研究成果をあげています。ここでは、研究室としての取り組みを伺うと共に、加藤忠史教授、西岡将基准教授、窪田美恵特任准教授それぞれの研究についても紹介していただきました。
双極性障害の治療法確立に向けて基礎・臨床の両面から研究

加藤忠史 教授
双極性障害は、精神疾患の中でも頻度が高く、統合失調症と並ぶ“二大精神疾患”とされています。かつては躁うつ病と呼ばれ、ほとんど眠らずに動き回るなどの躁状態と、興味や喜びが喪失するうつ状態という極端な状態を行ったり来たりする病気です。リチウムなどの気分安定薬を服用すれば症状の予防・改善が望めますが、リチウムは副作用が多いため治療を中断したり、病気をなかなか受容できなかったりして、再発を繰り返してしまいます。
双極性障害の原因としては、遺伝的要因が大きいと考えられます。また、双極性障害の躁状態、うつ状態に脳の機能の変化が関係していることは明らかです。しかし、 “こころの病”という偏見にさらされることが多く、人間関係のトラブルから社会生活に困難を抱えることになるのです。治療薬も偶然に近い形で発見されたものや、ほかの病気のために開発された薬の転用しかない状態にあります。
双極性障害の患者さんの脳内で起きていることを知りたいと思っても、生きたままの脳を直接調べることはできません。病気を再現するモデル動物もない中で、私たちは病気の原因を解明するための研究をしてきました。脳内の病態が明らかになれば、そこに直接作用するような新たな治療薬がつくれるはずです。
患者さんのMRスペクトロスコピー(MRIを用いて生体内の代謝物質の構造などを調べる手法)所見や死後脳の観察などから、脳内でミトコンドリア機能障害が起きていることに着目しました。ミトコンドリア機能障害により多彩な症状があらわれるミトコンドリア病でも中枢神経症状として双極性障害が出ることがありますから、そこに重要なヒントが隠されていると考えました。そこでミトコンドリア病の中枢神経症状のモデルマウスを作製したところ、反復性のうつ症状が出現し、患者さんに投与すると同状態を引き起す種類の抗うつ薬を投与すると躁状態のような行動変化が現れることを見出しました。
細胞内小器官であるミトコンドリアは、ATPなどのエネルギー生成をすることが知られています。この機能が失われると、糖尿病や心筋症、筋力低下など全身のあらゆる臓器で障害が生じます。パーキンソン病についても、ミトコンドリアが原因の1つだとされています。となると、次に重要になるのは、ミトコンドリア異常が起きている脳部位を見つけることです。そこから約10年の歳月をかけて、脳内の視床室傍核(PVT)という部位でミトコンドリア異常が蓄積していることを発見しました。
視床室傍核のミトコンドリア機能異常という研究ターゲットができてからは、死後脳による研究と、双極性障害の発症に関わる原因遺伝子の探索に取り組んでいます。双極性障害の患者さんとその家族のDNAを用いたエクソーム解析(全ゲノムのうちタンパク質のアミノ酸配列を決めている部分の解析)では、双極性障害患者さんで多くの変異を発見しています。
次は、この“視床室傍核仮説”にもとづいて、いよいよ臨床的な精神医学に切り込みます。約20年間にわたって基礎研究を続けていた理化学研究所から順天堂大学にやってきたのは、そのためです。さまざまな診療科の医師やメディカルスタッフが働く順天堂医院という臨床現場で、患者さんのデータに触れることができるこの環境は、病気への理解を深めて新しい治療法をつくりだす上で理想的といえます。
学内の連携では、放射線科との共同で患者さんの視床室傍核の機能的・構造的変化を可視化する研究を進行中で、良好な結果をあげています。また、ゲノム・再生医療センターの協力を得て、iPS細胞を使った研究も始めました。
今後も視床室傍核仮説を中心として、あらゆる角度から双極性障害の病態を研究し、より良い治療法の確立を目指していきます。

左から:西岡将基 准教授、加藤忠史 教授、窪田美恵 特任准教授
ゲノム解析とシングルセル解析で分子レベルでの病態解明に貢献する

私は精神科医として、10年ほど精神疾患の診療にあたってきました。その中で、診断が曖昧で主観的な要素が強い精神医学の状況に不十分さを感じ、生物学的な基礎研究に興味を引かれるようになりました。基礎研究に転じてからは、ゲノム解析研究を中心に行うことで精神疾患の遺伝的要因を明らかにしようとしています。(西岡将基 准教授)
双極性障害の研究では、網羅的なゲノム解析を行うことで、これまでの仮説やそれとは異なる病態のメカニズムが明らかになると考えています。ゲノム解析で特に注力してきたエクソーム解析(全ゲノムのうちタンパク質のアミノ酸配列を決めている部分の解析)では、両親にはなく子どもだけに検出される突然変異(デノボ変異)を中心に調べてきました。
また、従来の双極性障害研究では、親から子に受け継がれる生殖系列の遺伝因子について調べられてきましたが、私は受精卵から発生・発達する過程で生じる体細胞性のモザイク変異(一部の細胞だけに検出される変異)について解析をしています。2023年に発表した研究は、235名の双極性障害患者さんと39名の対照者の唾液や血液などの末梢試料からDNAを抽出して行いました。その結果、双極性障害患者さんには発達障害の原因遺伝子上にタンパク質の機能を障害するようなモザイク変異が多いことがわかりました。さらに、同じようにミトコンドリアゲノムについても解析を行ったところ、ミトコンドリアのトランスファーRNA上にヘトロプラスミー変異(一部のミトコンドリアDNAだけにあらわれる変異)が検出されました。
ゲノム解析と並ぶもう1つの研究アプローチとして、脳シングルセル解析に注力しています。シングルセル解析とは、細胞集団ではなく個々の細胞を1つずつ解析して細胞の性質を決定する解析手法です。この技術によって、従来とは異なる次元で細かく分子・細胞の脳病態を観察することが可能になりました。脳の病態を観察する手法としては、非常に大きなブレイクスルーとなる方法であり、シングルセル解析によって、精神疾患の脳病態を明らかにしていきたいと考えています。
これらの研究を通して、双極性障害の分子細胞病態を明らかにして、双極性障害の新たな治療シーズを発見したいですね。


モデルマウスや死後脳を用いて新しい治療薬につながる化合物を探索
私は、双極性障害のマウスモデルの開発やミトコンドリアをターゲットとする化合物スクリーニング法の開発などに携わってきました。マウスとヒトの生物学的な共通点を利用して、基礎から臨床へと橋渡しするトランスレーショナルな評価系を開発し、創薬につなげられる研究を行っています。(窪田美恵 特任准教授)
具体的には、マウス脳から単離したミトコンドリアを用いてミトコンドリアのカルシウム取り込み能を測定し、取り込み能を亢進させる化合物をスクリーニングしています。背景として、双極性障害の患者さんの細胞では、カルシウム濃度が上がりやすい傾向があるという報告があります。そこで、ミトコンドリアがより多くのカルシウムを取り込むようにすれば、細胞質のカルシウム濃度の上昇量を抑制することができると考え、異常な細胞の状態を正常に戻す働きを示す化合物を探索しています。

また、脳特異的にミトコンドリア障害を発症する気分障害モデルマウスの開発も、重要な研究テーマの一つです。このマウスに長期の輪回し行動をさせると、輪回し行動量が一時的に低下して、うつ症状が見られます。このような異常行動を示すモデルマウスに、気分安定薬として使われているリチウムやエスシタロプラムなどを投与すると、症状が改善することがわかりました。現在、この気分障害モデルマウスを用いて、これまでにスクリーニングした化合物が行動レベルでも効果を示し、異常行動を抑制するかどうかを検証する研究を行っています。
さらに、海外のブレインバンクから入手した双極症患者さんの死後脳を用いて、ミトコンドリア障害仮説を検証する研究も行っています。この研究では、視床室傍核に注目して、モデルマウス同様に視床室傍核でミトコンドリア障害を持つ細胞が多いかどうかを調べています。
このようにモデルマウスから死後脳までを用いてミトコンドリア障害を検証し、脳内の原因部位を同定することで、より病態の理解を深めることが可能になり、病態に基づいた治療薬の開発へつなげることができると考えています。
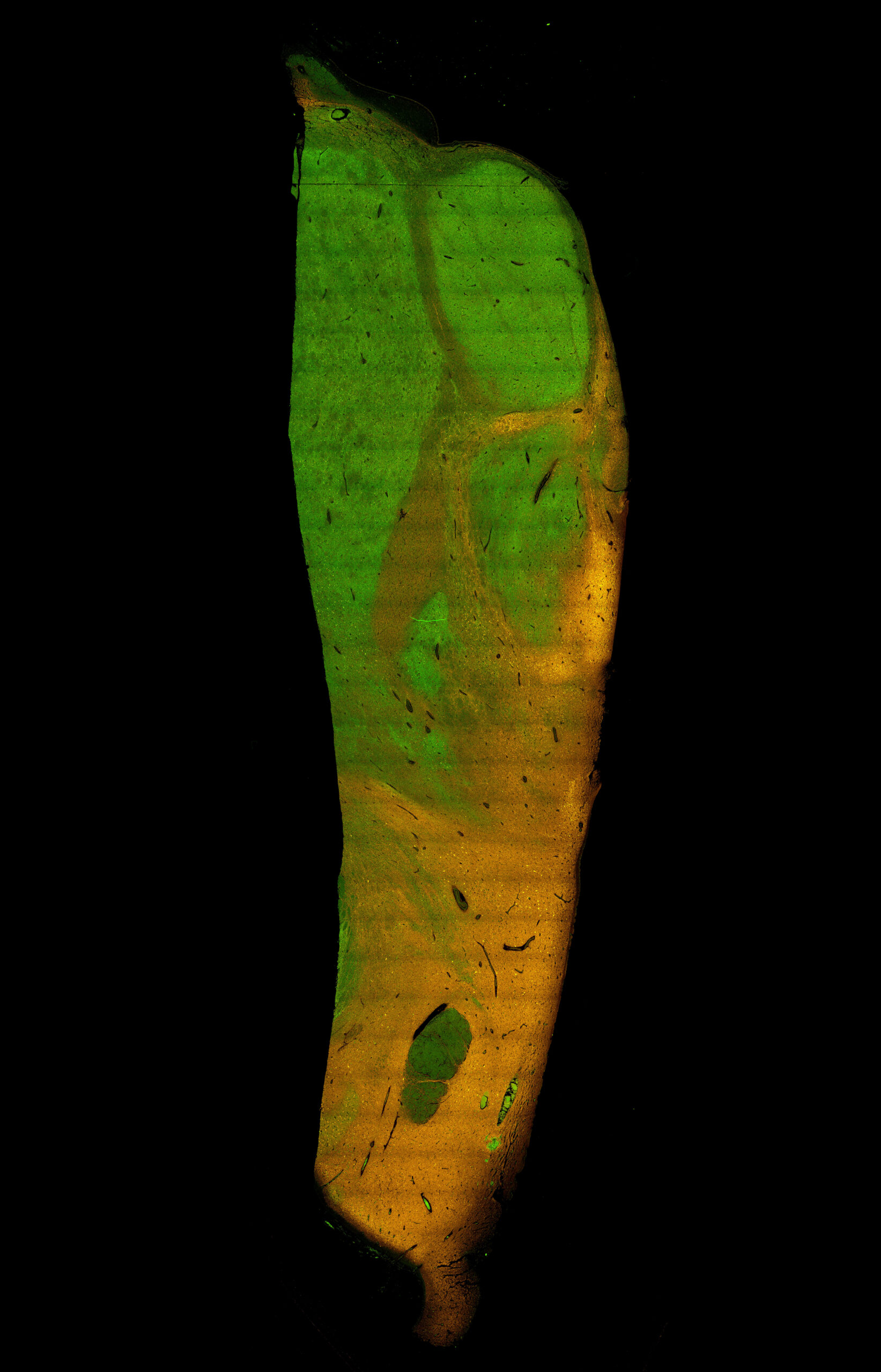
【左図】
ヒト死後脳のホルマリン固定後のパラフィン包埋切片(視床室傍核を含む視床の一部)。
右:内側、左:外側、上:背側、下:腹側
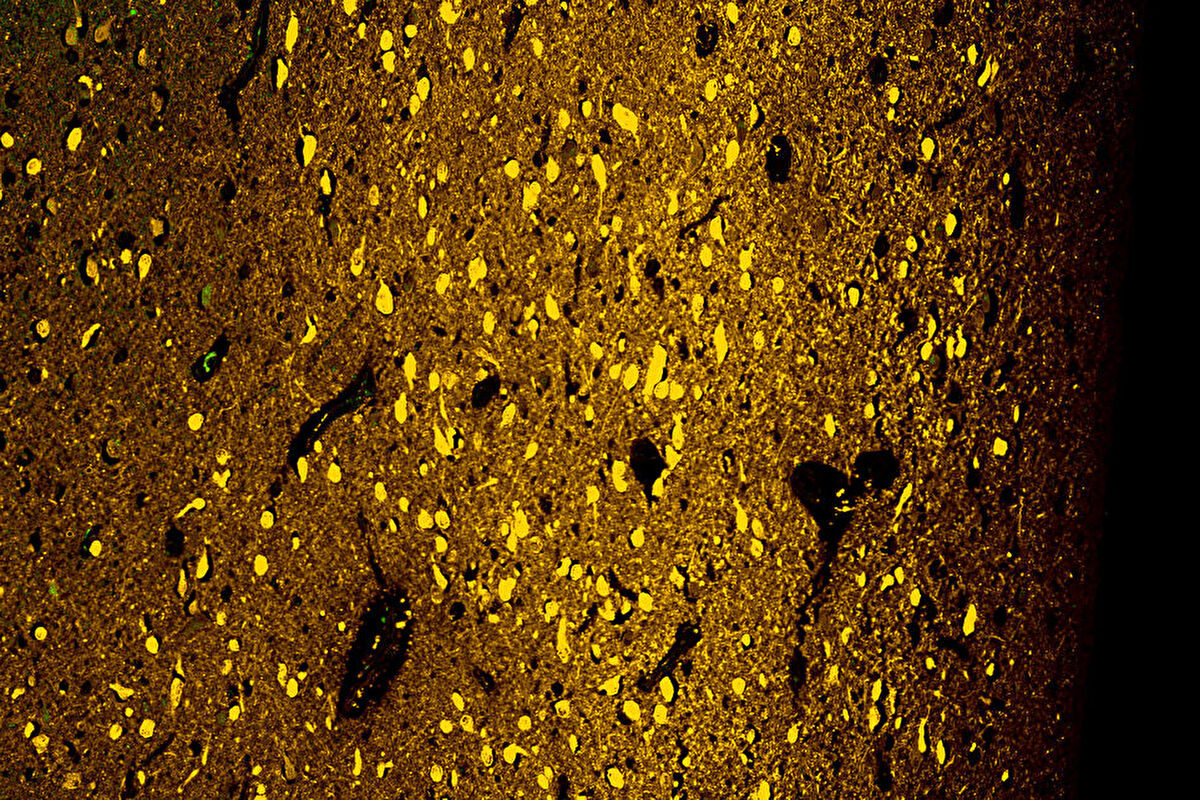
【上図】
左と同じ切片の拡大像(Ⅹ20):カルレチニン抗体を用いた免疫組織化学染色(黄色~橙)。視床室傍核と想定される領域に多く染まっていることがわかる。
双極性障害の病因解明がライフワーク
生物学的精神医学を確立する
双極性障害をライフワークとして、約35年間にわたって、臨床医学、基礎医学の両面からこの病気の病因解明に努めてきました。そのうちの20年間を理化学研究所での基礎研究に費やし、ミトコンドリア障害仮説にもとづいて視床室傍核を原因部位のターゲットに定めるなど、さまざまな成果をあげてきました。
順天堂大学では、①世界標準の精神医学的診断・治療を提供する、② 仁の心・科学する心を持ち、生涯社会貢献できる精神科医、及び精神医学を理解し活用できる医師を育成する、③ 未来の精神医学を創る先端的研究を行う、という3つのミッションを掲げています。これらのもと、一人ひとりが自らのモチベーションでやりがいを持って仕事ができる環境をつくっていきます。
2020年9月1日には、双極性障害をはじめとした気分障害の診断法・治療法開発の推進を目的とした気分障害センターを設置しました。この中で双極性障害の専門外来を開設して、「双極性障害治療立て直し入院」プログラムを行っています。双極性障害治療立て直し入院は、2週間の入院期間にさまざまな検査を行い、診断・治療の見直しをすることで、症状の改善や予防を目指すものです。
研究面では、住友ファーマとの共同研究講座「気分障害分子病態学講座」を開設しました。この共同研究講座では、①双極性障害患者死後脳における視床室傍部病変の検討、②死後脳の単一神経核RNAシーケンスによるヒト視床室傍核セルタイプの同定、③双極性障害における視床室傍核を巡る神経回路の病態の解明、④視床室傍核異常に着目した創薬研究という4つの研究テーマを中心に取り組んでいます。
こうした一連の研究が、精神疾患の病因を分子・細胞レベルから神経回路・行動レベルまで理解する、生物学的精神医学分野における成功した研究プロジェクトの一つになると確信しています。次の段階では、これらの研究成果を臨床につなげることを目標に、基礎医学と臨床医学を統合しながら、研究を推進していきます。

研究者Profile

加藤 忠史
Tadafumi Kato
医学部精神医学講座/大学院医学研究科精神・行動科学
教授
【関連記事】ミトコンドリアの異常に着目し双極性障害の病態解明に迫る
【関連記事】双極性障害の病態を明らかにして精神疾患の診断・治療に革新をもたらす
Researchmap
研究者Profile

西岡 将基
Masaki Nishioka
医学部精神医学講座
准教授
Researchmap
研究者Profile

窪田(坂下) 美恵
Mie Kubota-Sakashita
大学院医学研究科気分障害分子病態学講座/医学部精神医学講座
特任准教授
Researchmap




