ヒトの体内には、数十兆個の細胞があります。その一つひとつに「オルガネラ」と呼ばれる小器官があり、さまざまな働きをしています。このオルガネラが機能不全になると神経系を始めとする様々な臓器の疾患につながります。神経系では手足の自由が奪われるパーキンソン病はその代表例です。大学院医学研究科神経機能構造学の小池正人教授は、神経細胞におけるオルガネラの機能破綻のメカニズムを解明し、パーキンソン病を始めとする神経変性疾患の治療に役立てようとしています。
細胞内小器官の異常が神経変性疾患に関与している
私の研究対象は、細胞内の「オルガネラ」です。「細胞内小器官」と呼ばれる組織の総称で、細胞核、小胞体、ゴルジ体、リソソーム、ミトコンドリアなどがこれにあたります。私たちの体内は、200以上の種類に分化したさまざまな細胞から構成されており、その総数は数十兆個と考えられています。その細胞一つひとつの中で、オルガネラが個々の働きをして、私たちの身体が成り立っています。
例えば、ミトコンドリアは細胞のエネルギーとなるATP(アデノシン三リン酸)を産生し、ゴルジ体は細胞内の分子を適切な場所に運ぶ役割を担います。そして、リソソームは細胞内外の物質や自身の細胞のオルガネラを取り込んで分解する“細胞の胃袋”のような働きをしています。これらのオルガネラの機能不全が老化やさまざまな疾患の原因となることがこれまでの研究でわかっています。
オルガネラの機能破綻、すなわち「オルガネロパチー」が、パーキンソン病やアルツハイマー病などの神経変性疾患に関与しているのではないかと考え、研究を進めています。

オルガネロパチーとパーキンソン病
ここでは代表的な神経変性疾患であるパーキンソン病を例に詳しく説明しましょう。手足が自由に動かなくなり、震えなどの症状も出るパーキンソン病は、中脳黒質と呼ばれる場所の神経細胞の変性によって、脳内のドパミンが減少することで引き起こされると考えられています。パーキンソン病には、孤発性と遺伝性のタイプがあり、遺伝性のものだけでも現在20以上発見されています。
その原因遺伝子産物の同定を通して、ミトコンドリアやリソソーム、小胞体などのオルガネラの異常が、中脳黒質の神経細胞の変性に関わっていることがわかってきました。しかも細胞内の個々のオルガネラの異常だけでなく、オルガネラ同士の連携の破綻が関与している可能性もあります。詳しくは後述しますが、現在は、パーキンソン病と関連する黒質の神経細胞のオルガネロパチーに焦点を当てて検討しています。
希少疾患の病態解明の知見をパーキンソン病の研究につなげる
私は大学院時代から、オルガネラに関する研究に従事してきました。当時は、細胞内のリソソームのタンパク質分解酵素の欠損による神経変性疾患の研究をしていました。リソソームの構造や機能に関わる遺伝子の変異などによって引き起こされる様々な希少疾患が「ライソゾーム病」(ライソゾームはリソソームと同義)と総称されております。
私どもが研究の対象としたライソゾーム病では、ミトコンドリアのタンパク質が分解されずにリソソームに蓄積されます。ここには、ミトコンドリアのオートファジーの異常が関与しています。オートファジーとは、細胞の「自食作用」などと表現される自己成分を分解する機能のことで、ミトコンドリアのオートファジーは、「マイトファジー」と呼ばれています。
このマイトファジーの分子メカニズム解明の研究が、パーキンソン病の病態解明につながっていきます。例えば、順天堂大学で発見されたパーキンソン病の原因遺伝子産物perkin(パーキン)が、マイトファジーに関与していることが海外のグループにより明らかにされました。さらに、本学神経学講座との共同研究によって、ある種の遺伝性パーキンソン病の病態が私どもが研究していたライソゾーム病と極めて似ているという事例を見出しております。
これらの知見は、私どもが研究してきた希少疾患であるライソゾーム病の病態理解が、パーキンソン病の研究にも役立つことを示唆しています。オルガネロパチーに伴う個々の神経変性疾患は希少なものですが、その病態メカニズム解明を通して得られた知見を今後はより一般的な疾患の病態メカニズム解明に応用していくつもりです。

iPS細胞を用いた新たな実験方法に挑戦
前述した通り、オルガネロパチーには、細胞内のさまざまな構造変化が関与しています。これを正確に評価するためには、光学顕微鏡だけでなく、電子顕微鏡を用いた形態観察が必要です。電子顕微鏡解析は個別の細胞内小器官の解析にとどまらず、細胞内小器官の相互関係、例えば、ミトコンドリアと小胞体の接触などの評価にも有用です。そのため、光学顕微鏡から電子顕微鏡レベルまで、シームレスに解析するための各種相関観察法の利用や技術開発を行っております。オルガネラの研究を進める上で、順天堂大学の実験環境には大いに助けられています。
さらに免疫電子顕微鏡法によって、オルガネラの分子の局在を詳細に観察することも可能です。私は細胞生物学領域でよく用いられてきた凍結超薄切片法(徳安法)と呼ばれる解析方法を専門としており、オランダのユトレヒト大学に客員教授として留学し、オートファジー関連分子の可視化に関する研究を行った経験もあります(上画像:徳安法により切り出されている切片(画面中央))。
パーキンソン病の病態解明に関しては、最近iPS細胞を用いた実験にも挑戦しています。私たちの研究室では、オルガネロパチーの研究にあたり、主としてモデルマウスを用いた解析を行ってきました。しかし、パーキンソン病のモデルマウスでは、ヒトの中脳黒質の神経細胞の特異的な変性を再現するものは稀です。そこで、本学のゲノム・再生医療センターとの共同研究で遺伝性パーキンソン病の患者由来のiPS細胞を中脳黒質のドパミン神経細胞に分化させ、健常者のものと比較検討する方法を考えました。これにより、ドパミン神経細胞における細胞種特異的なオルガネロパチーを捉えたいと考えました。
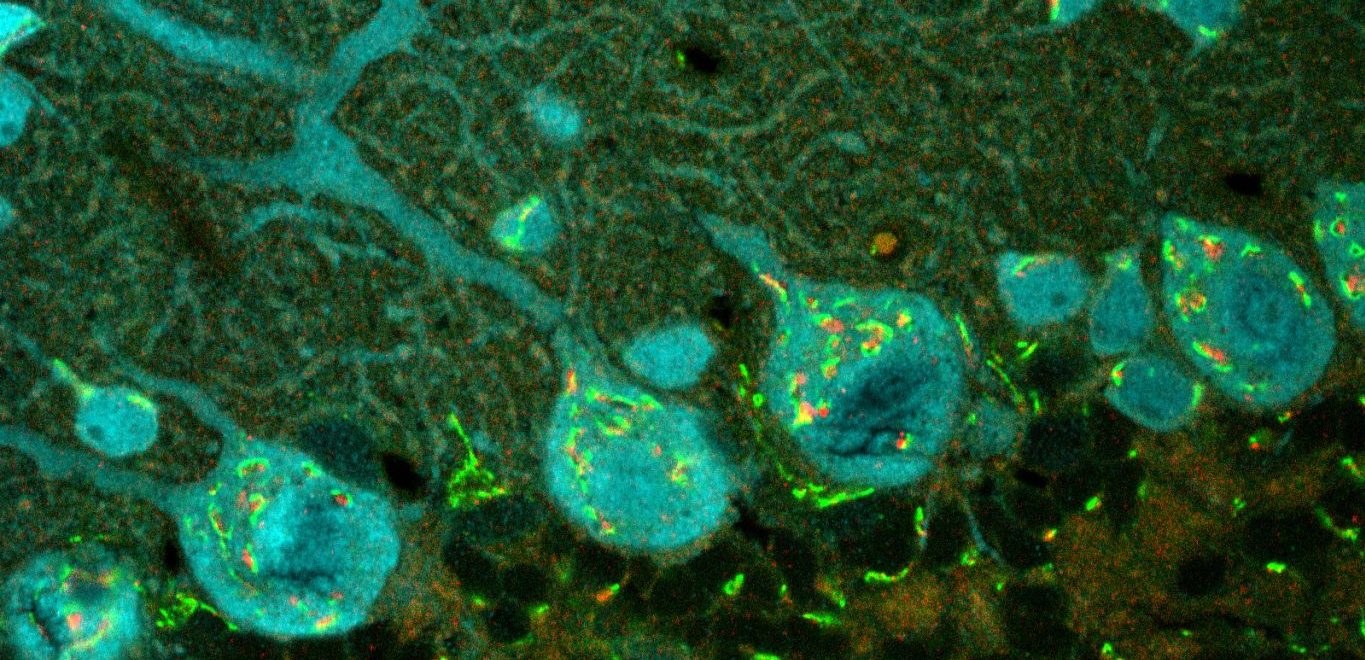
しかし、現状では全てのiPS細胞をドパミン神経細胞分化させることはできません。必ず他の細胞が紛れ込みます。そこで、ドパミン神経細胞への分化によってGFP(蛍光タンパク質)を発現するiPS細胞を新たに作成し、光顕−電顕相関観察法(CLEM)という手法によって、GFPが光っているドパミン神経細胞を狙い撃ちして電子顕微鏡で観察する流れを確立しました(下画像:iPS細胞由来のドパミン神経細胞)。
これによって、中脳黒質のドパミン神経細胞では、健常者においても他のタイプの神経細胞と比べてミトコンドリアの構造機能が異なるなどの新たな知見も明らかになりました。さらに、ミトコンドリアのストレス時の応答が、パーキンソン病患者と健常者のドパミン神経細胞で異なることもわかりました。

パーキンソン病研究の最先端拠点である強みを活かす
これまでは、モデルマウスやiPS細胞を用いた電子顕微鏡レベルの形態観察が中心でしたが、現在新たに作成したドパミン細胞でGFPを発現するiPS細胞を用いて、分子レベル、遺伝子レベルの解析を進めており、健常者と患者由来ドパミン細胞でのオルガネロパチーに関係する遺伝子発現の差異が見いだされてきました。パーキンソン病におけるドパミン細胞特異的なオルガネロパチーの解明が進めば、関連する分子の機能の制御などを通した治療法開発につなげることも可能でしょう。
順天堂大学は、パーキンソン病研究の最先端拠点です。学内の研究室と連携しながら、オルガネロパチー研究の知見をパーキンソン病を始めとする神経変性疾患の病態メカニズムの解明につなげていきたいと思っています。
研究者Profile

小池 正人
Masato Koike
大学院医学研究科神経機能構造学
教授
Researchmap